搜索


近日,EON体育4平台陳海峰教授課題組在J. Chem. Theory Comput. 期刊在線發表題為“Well-balanced Force Field ff03CMAP for Folded and Disordered Proteins”的研究成果🧑🏿🏭,提供了一種新的高效而平衡的🏄🏼♀️、能夠同時模擬結構蛋白和天然無規蛋白的分子力場。碩士生張陽鵬為第一作者👶🏿,陳海峰教授為通訊作者。
蛋白質是生命的物質基礎👨🏼🦰,蛋白質有結構蛋白和天然無規蛋白兩種類別👡。天然無規蛋白是一類在生理條件下沒有穩定三級結構的蛋白質,這類蛋白在真核生物蛋白質組中的含量超過40%,與腫瘤、心血管疾病、神經退行性疾病以及糖尿病等復雜疾病的發生發展密切相關🔚。結構蛋白的序列結構功能範式已經被大家廣泛接受👷♂️,但天然無規蛋白的序列無規功能範式迫切需要建立🥓。與結構蛋白相比🧑🏿💼,天然無規蛋白構象多樣性等特點導致難以用X-ray、NMR等傳統實驗方法來研究👮🏼♂️。分子動力學模擬是研究天然無規蛋白的序列無規功能範式的重要方法🐾,分子力場是分子動力學模擬的基礎🧑🦽➡️,但現有的分子力場尚不能同時模擬結構蛋白與天然無規蛋白。因而,依賴於高性能計算的分子動力學模擬在天然無規蛋白的研究中發揮著越來越重要的作用。
由此💆🏿🤣,陳海峰教授課題組在ff03分子力場的基礎上,通過添加基於能量的矯正項,發展了一種平衡而高效的分子力場ff03CMAP,為天然無規蛋白的序列無規功能範式的建立奠定了堅實基礎🕴🏻⚒。通過對短肽、天然無規蛋白、結構蛋白以及快速折疊蛋白等的大量測試結果表明,該分子力場模擬的化學位移、J-耦合,序參數以及殘基偶極耦合都與NMR試驗觀察高度一致,同時比其它分子力場的模擬結果更加準確🧘🏼。
該分子力場的發布對於揭示天然無規蛋白的序列無規功能範式以及基於天然無規蛋白的復雜疾病發生發展的分子機製都具有重要的意義🏊🏿♀️。
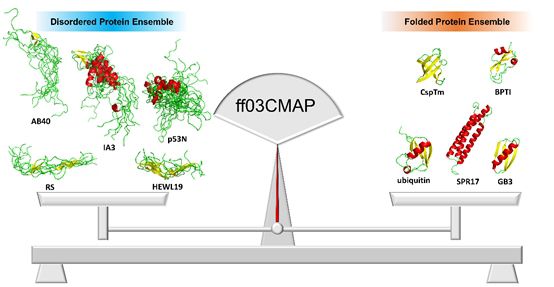
該研究獲得國家重點研發計劃以及國家自然科學基金面上項目的資助。
論文鏈接:https://pubs.acs.org/doi/10.1021/acs.jctc.9b00623


 首頁
首頁

 EON4概況
EON4概況

 師資隊伍
師資隊伍

 人才培養
人才培養

 招生就業
招生就業

 科學研究
科學研究

 平臺基地
平臺基地

 黨群工作
黨群工作

 校友之家
校友之家

 安全工作
安全工作

 網上辦事
網上辦事

 當前位置:
當前位置: