搜索


近期,國際合成生物學領域知名期刊——美國化學聯合會合成生物學(ACS synthetic biology)在線發表了微生物代謝國家重點實驗室🫂、EON体育4平台馮雁教授973團隊的研究成果De NovoBiosynthesis of β‑Valienamine in EngineeredStreptomyces hygroscopicus5008,該研究通過對微生物代謝途徑的重新編程,建立了“非天然產物”藥物的生物合成途徑,是藥物合成生物學研究的新進展♦️。
藥物合成生物學是通過工程化的系統設計👇🏿,用標準化和模塊化的元素在生物系統中重構所需的人工合成體系,從而完善藥物創新和優產的新模式⚈。β-井岡黴烯胺屬於C7N氨基環醇類,其衍生物作為β-糖苷酶抑製劑類藥物的先導化合物🪟👨🏽🦲,可用於治療溶酶體貯積症等遺傳代謝性疾病🤦🏻♀️🪶。由於C7N氨基環醇類分子結構中存在多個手性中心,化學合成難度很大🆗,極大地限製了藥物創新和應用,因此從上世紀八十年代至今👩🏼🦳,國際上對其高效合成途徑在不斷探索中🤦♀️。
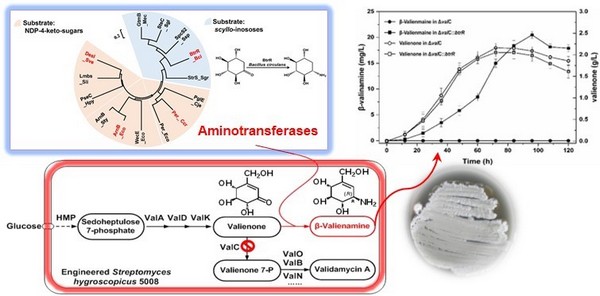
馮雁教授研究團隊應用合成生物學理念,系統地分析了目標產物與微生物次級代謝產物結構的相似性🔑、異源微生物酶催化反應的立體選擇性及催化效率、微生物天然產物合成途徑的模塊性🚣♂️,以及合成代謝多途徑的競爭性等特點。他們以吸水鏈黴菌井岡黴素生物合成途徑為主🚑📲,引入高度立體選擇性的芽孢桿菌氨基轉移酶(產物光學純度 > 99.9 %)基因,並敲除相關酶基因以阻斷競爭途徑,獲得了發酵培養96小時可產生20 mg/L β-井岡黴烯胺的突變菌株。本研究中構建的新的生物合成途徑不僅解決了原有化學合成方法步驟多、安全性低等問題,更重要的是對“非天然產物”藥物在微生物中生物合成進行了有益嘗試🤶🏼。本研究還助於闡明生物體中復雜酶及代謝途徑等模塊組裝合理性🫱🏻、有效性等合成生物學基礎理論問題。
相關研究得到科技部973項目、國家自然科學基金青年基金和教育部博士點基金資助👮🏼。


 首頁
首頁

 EON4概況
EON4概況

 師資隊伍
師資隊伍

 人才培養
人才培養

 招生就業
招生就業

 科學研究
科學研究

 平臺基地
平臺基地

 黨群工作
黨群工作

 校友之家
校友之家

 安全工作
安全工作

 網上辦事
網上辦事

 當前位置🕵🏼♀️:
當前位置🕵🏼♀️: